两种金属粉末的混合物30 g,与足量的稀硫酸反应,只生成氢气1 g,则这种混合物中的两种金避可能是( )
A.Mg和Al B.Zn和Fe C.Mg和Fe D.Al和Fe
审题与思路:由题意可知,题中提供的金属有四种,它们与稀硫酸反应的化学方程式如下:
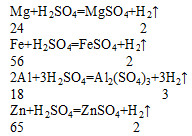
2 无论是哪一个化学方程式,我们都可以使氢气前的化学计量数为1,使氢气下面对应的相对分子质量均为“2”。这样我们不妨设金属混合物的化学式为R(在其化合物中显+2价),其平均相对原子质量为X,则有:
R+2HCl === RCl2+H2↑
x 2
30 g 1 g
![]()
即得金属混合的的平均相对原子质量为60。 由题目所提供的答案我们可以分析出答案为B,因为对于A来说Mg的相对原子质量为24,Al的相对原子质量虽为27,但当氢气下的相应相对分子质量为2时,我们可以把Al的相对原子质量看成是18。而24和18相混合,所得的平均相对原子质量只能是大于18且小于24。
如此类推,B中Zn、Fe的相对原子质量分别为65、56,则它们混合后所得的混合的的平均相对原子质量为小于65且大于56的数。题中x平均相对原子质量正好在这一数当中,故选B。
C中,Mg、Fe相混合后,平均相对原子质量应为一个小于56且大于24的数;D中Al、Fe相混合,其平均相对原子质量为一个小于56且大于18的数。
注意:①要理解Al的相对原子质量应为27,为什么这里说可以看作为18。②Al与酸(稀盐酸、稀硫酸)反应的化学方程式很容易出错。
解答:选B
总结:抓住题目中所提供的物质的反应特征,抓住平均相对原子质量和平均相对分子质量的实质,然后解题,可收到事半功倍的效果。
tag: 技巧 选择题 中考化学 平均值中考化学复习资料,中考化学复习资料大全,初中学习 - 中考复习 - 中考化学复习资料